
2021年7月发表在《LeukemiaLymphoma》期刊上的一篇文章,介绍了多发性骨髓瘤(MM)和轻链型(AL)淀粉样变性的治疗进展,高效治疗方法的出现已使治愈变得可能。关键是需要一种高度灵敏的可测量残留病变(MRD)技术来取代传统的反应评估。越来越多的研究将MRD作为研究终点,证实了MRD既是治疗反应的预测标志物,也是疾病复发的预后标志。本综述对MRD的相关内容进行了重点分析,包括目前支持在临床实践中使用MRD的证据,检测MRD各种方法的优缺点,并指出了检测MRD的指征和目前临床试验需要解决的问题。具体内容如何,小编带大家了解一下。
背景
MM和AL淀粉样变性的治疗在不断进展,新的治疗方法的出现使治疗结局得到改善。新疗法的引入带来了非常高的完全反应率(CR),引发思考疾病治愈的可能性。评估反应深度需要高度灵敏的方法来检测残留的肿瘤细胞。微小残留病(MRD)被定义为治疗后持续存在且无法通过常规血清学方法检测到的肿瘤细胞数量。
MRD的检测方法
1.骨髓(髓内)MRD
目前骨髓MRD检测的标准化方法包括二代流式细胞术(NGF)和二代测序法(NGS)(表1)。NGF是评估MRD的标准化方法,灵敏度高,适用范围广。NGF可以通过细胞表面标记物区分正常和异常浆细胞,并基于Euroflow指南和IMWG共识标准,使用2管8色抗体面板(CD138,CD27,CD38,CD56,CD45,CD19,CD117,CD81,κ和λ轻链)进行检测。NGS是一组利用DNA测序来评估MRD的方法[深度测序、等位基因特异性寡核苷酸定量PCR(ASO-qPCR)、高通量测序等]。深度测序已得到验证,与NGF和ASO-qPCR有良好的一致性,MRD阴性患者的OS和下一次治疗(TTNT)时间更长。
2.骨髓外MRD(影像学和外周血)
尽管骨髓内MRD阴性,但仍可能存在髓外疾病。用于MRD检测的PET-CT已纳入IMWG指南,并可预测无进展生存期。PET-CT最近已被标准化用于MM和抗浆细胞治疗后,局部病灶以及骨髓FDG摄取量低于肝脏背景值(Deauville量表4)的MRD检测,可预测更长的OS和PFS。磁共振弥散加权成像(DW-MRI)是一种功能性磁共振成像,它根据水分子运动的差异显示组织之间的对比(相对于评估代谢活动的PET-CT)。其主要优点是可以检测到弥漫性骨髓浸润,由于骨髓增生导致的假阳性率相对较低。免疫-PET是一种很有前景的新型MRD成像方法。在10名患者中对其效果进行了评价,结果显示是敏感的,但它在MRD评估中的临床作用仍不清楚。

MM中的MRD
1.NDMM(初诊多发性骨髓瘤)
几项研究评估了MRD在接受三联疗法和四联疗法治疗NDMM患者中的作用(表2)。
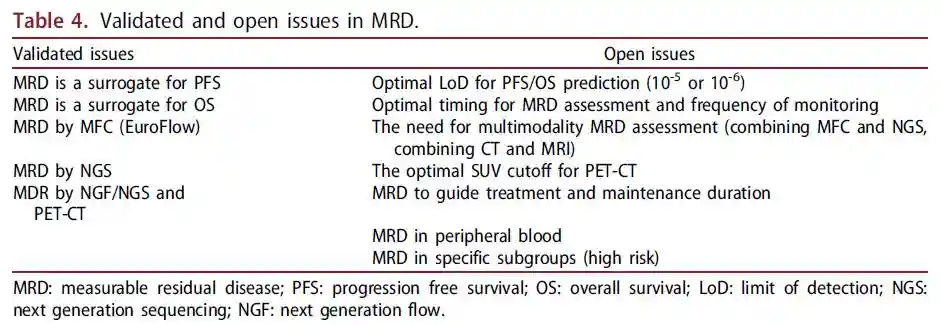
三联疗法
URANCE试验:MRD作为研究次要终点,MRD阴性率(NGF,LoD10-6)在VRd组为7%,在KRd组为10%(p=0.079)。
FORTE试验:2期FORTE试验是一项以MRD作为次要终点的研究。本试验比较了76例患者的KRd、KRd/ASCT和KCd/ASCT,并采用了两种方法进行MRD评估:NGS(LoD10-5)和NGF(LoD10-5)。两种方法NGS和NGF获得的MRD阴性率不一致,分别为14%(LoD10-5)和21%(LoD10-6)。
MAIA试验:针对不适合移植NDMM患者,12,18,24和30个月时在达到CR患者中进行MRD(NGS,LoD10-5)检测,DRd组的MRD阴性率较对照组更高(24.2%)。MRD对PFS有预测作用。
CLARION试验:MRD阴性率在KMP和VMP间无差异(15.7%%)。
四联疗法
GRIFFIN研究:一项评估Dara-VRd与VRd的关键性3期研究。MRD(NGS,LoD10-5)作为研究次要终点。D-VRd组MRD阴性率明显较高,并且在ASCT后比率进一步增加。
CASSIOPEA试验:在1085名符合移植条件的患者中比较了Dara-VTd与VTd,发现Dara-VTd组的MRD阴性率(NGF,LoD10-5)更高(64%%),且NGS和NGF之间具有良好的相关性。
MASTER研究:首个报道的采用四联疗法、根据MRD调整治疗NDMM的研究。使用NGS(LoD10-5)评估多个终点的MRD。ASCT/4周期巩固治疗/8周期巩固治疗后达到MRD阴性的患者停止治疗,并进行MRD监测。ASCT后MRD阴性率增加(诱导后42%,ASCT后73%),但需要更长的随访时间验证缓解是否会持续。
ALCYONE研究:706名不符合移植条件的患者被随机分配到Dara-VMP与VMP,Dara-VMP组的MRD阴性率较高(28%%)。Dara-VMP组的持续MRD阴性率(在6和12个月时评估)[NGS(LoD10-5)]也较高。MRD对PFS和OS有预测作用。
自体干细胞移植(ASCT)
ASCT被认为是符合移植条件NDMM患者的标准治疗方法,3期试验均支持移植相比常规新疗法可改善患者PFS。在高效诱导方案时代,目前正在临床试验中评估使用MRD阴性来指导推迟ASCT决策,如2期ADVANCE试验(NCT04268498),根据初始治疗后的MRD状态,随机选择早期或延迟移植治疗。
2.RRMM
几项研究评估了MRD在RRMM中的作用。
POLLUX试验:DRd组的MRD阴性率较高(30.4%%),随着随访时间的延长,反应加深。
CANDOR试验:DKd组在12个月时具有更高的MRD阴性率(NGS,LoD10-5)
ICARIA试验:在Isatuximab、泊马度胺和地塞米松(Isa-Pd)组中,MRD阴性率为5%,在泊马度胺和地塞米松(Pd)组中为0%。
BELLINI试验:接受Venetoclax、硼替佐米和地塞米松治疗患者具有更高的MRD阴性率(NGS,10-5)(15%%),及更高的持续1年MRD阴性率(7%%)。
CASTOR试验:与Vd组相比,DVd组的MRD阴性率更高。
3.SMM(冒烟型骨髓瘤)
目前正在研究SMM的早期干预方法,评估以治愈为目标的强化治疗方案,而不是以疾病控制为目标、不那么积极主动的治疗方案。在GEM-CESAR研究中,纳入了90例具有移植资格的高危SMM患者,主要终点为MRD阴性(NGF)。诱导治疗后MRD阴性率为30%,ASCT后为52%,巩固治疗后为57%。中位随访32个月后,2%死亡,93%存活,无进展。
轻链型(AL)淀粉样变性的MRD
目前缺乏AL淀粉样变性的MRD数据,但有数据显示反应深度与结局相关。基于风险适应的临床试验、以及评估持续或强化治疗对MRD阳性患者作用的试验结果发现,MRD与器官反应之间存在相关性。还应对MRD作为AL淀粉样变性的替代试验终点进行探索,未来MRD可能会被纳入AL淀粉样变性的反应标准评估中。
临床实践中MRD评估的指征和未来研究
临床实践中使用MRD可预知患者预后。尽管MRD被纳入IMWG反应标准,但没有随机数据支持使用MRD阴性来改变维持治疗的时间、延迟ASCT或根据MRD结果调整治疗。临床试验中要进一步解决的问题是MRD评估时间、获得预测结果的最佳MRD组合,以及MRD是否可以用作监管药物批准的主要研究终点(表4)。
结论
MRD在MM和AL淀粉样变性中的应用还在不断发展中,越来越多的试验将MRD作为研究终点。MRD被证实具有较高的预后价值,检测越深入,预测能力越强。为避免过度治疗和治疗不足,需谨慎解释有关MRD的文献,还需考虑适用性、重复性和成本。研究人员需要合作收集数据和改变治疗模式。MRD只是针对特定病人制定治疗方案时应综合考虑的一个因素,而其他因素包括病人的特征(如合并症和表现状况)、疾病生物学(如FISH、rISS、髓外疾病)和治疗毒性(如骨髓抑制和神经病变),同样很重要。
参考文献:
1.VaxmanI,sis:;62(7):1544-1553.















